Ăn mòn điện hóa là gì?
Ăn mòn điện thế, một kẻ thù không đội trời chung trong thế giới vật liệu và kỹ thuật, nổi lên như một thách thức to lớn khi lựa chọn kim loại sai lầm va chạm. Nhiều người thấy rằng việc cố định các thành phần nhôm tại chỗ bằng bu lông hợp kim đồng là phù hợp. Nhưng như hình ảnh ở trên cho thấy, một vùng màu trắng bao quanh bu lông hợp kim đồng ở giữa xuất hiện trên nhôm liền kề. Ngoài ra, bu lông thép, khi không được kết hợp đúng cách với các tấm đồng, cũng bị ăn mòn Galvanic, để lại những vết gỉ sét khó coi. Trong bài viết này, chúng tôi sẽ khám phá nguyên nhân, tác động và khoa học đằng sau hiện tượng ăn mòn Galvanic và giải thích cách ngăn ngừa và xử lý hiện tượnGalvanic
Dãy thế điện
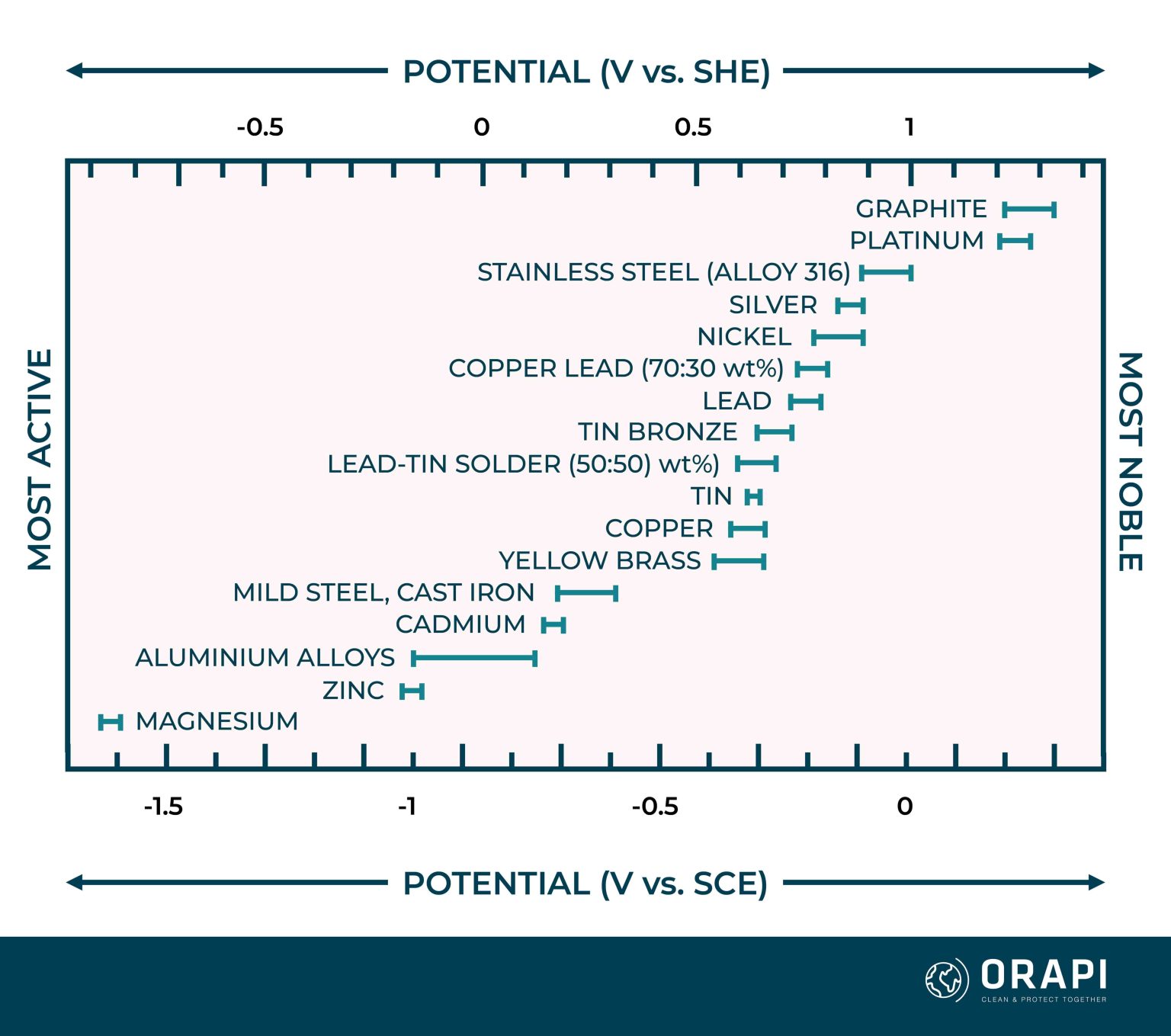
Các kim loại có thể được sắp xếp một cách có hệ thống theo dãy điện hóa, hỗ trợ đánh giá khả năng bị ăn mòn của chúng khi tiếp xúc. Dãy này, được trình bày chi tiết trong Bảng 1, thiết lập hệ thống phân cấp điện hóa của nhiều kim loại khác nhau, chủ yếu là trong nước biển. Đáng chú ý là mặc dù không phải kim loại, than chì dẫn điện đủ tốt để gây ra ăn mòn điện hóa và được đưa vào Bảng 1.
Dãy điện thế sắp xếp các kim loại từ kim loại phản ứng mạnh nhất (đầu dưới) đến kim loại phản ứng yếu nhất (đầu trên). Kim loại có thứ hạng thấp hơn trong dãy được coi là hoạt động mạnh hơn trong các cặp kim loại, trong khi kim loại có thứ hạng cao hơn là kim loại quý hơn. Khi hai kim loại tiếp xúc với nhau, kim loại hoạt động mạnh hơn dễ bị ăn mòn điện hóa. Ví dụ, kẽm tiếp xúc với thép mềm có thể bị ăn mòn vì kẽm hoạt động mạnh hơn thép mềm.
Bảng 1: Dãy điện hóa từ kim loại quý nhất ở đầu đến kim loại hoạt động mạnh nhất ở cuối.
Sự hình thành ăn mòn điện hóa
Để tạo điều kiện cho ăn mòn điện hóa, hai điều kiện phải được đáp ứng. Thứ nhất, các kim loại liên quan phải thiết lập kết nối điện, có thể đạt được thông qua tiếp xúc vật lý trực tiếp hoặc bằng cách sử dụng một môi trường dẫn điện khác, cho phép dòng điện chạy qua từ kim loại này sang kim loại kia. Thứ hai, chúng phải duy trì kết nối ion, cho phép dòng ion chảy giữa chúng. Điều này đòi hỏi phải có chất điện phân, thường là dung dịch chứa các ion, chẳng hạn như các ion có trong muối, axit hoặc bazơ hòa tan. Kết nối ion có thể được thiết lập khi các kim loại được ngập hoàn toàn trong chất điện phân hoặc khi chúng được phủ một lớp chất điện phân liên tục làm ướt cả hai kim loại một cách đầy đủ, một kịch bản thường được quan sát thấy trong điều kiện độ ẩm cao.
Khoa học cơ bản về ăn mòn điện hóa
Dòng điện hóa và khả năng ăn mòn
Hiện tượng ăn mòn điện hóa có thể được hiểu thông qua khoa học về thế ăn mòn và dãy điện hóa. Khi kim loại tiếp xúc với chất điện phân, nó trải qua một quá trình trong đó các nguyên tử của nó chuyển thành các ion và electron (e-). Ví dụ, hãy lấy sắt (Fe), phản ứng sau đây xảy ra:
Fe → Fe2+ + 2e−
Phản ứng này được gọi là phản ứng anot, dẫn đến sự hình thành các ion Fe2+. Đồng thời, các phản ứng khác trích xuất electron; ví dụ, oxy (O2) hòa tan trong chất điện phân có thể tham gia phản ứng tạo ra các ion hydroxide (OH−), như sau:
O2 + 2H2O + 4e− → 4OH−
Phản ứng này được gọi là phản ứng catốt. Các electron được chuyển vào kim loại trong phản ứng anot và được loại bỏ khỏi kim loại trong phản ứng catốt. Cân bằng đạt được khi các electron được lắng đọng và trích xuất với tốc độ tương đương.
Sự tương tác giữa các điện tích của ion và electron khiến kim loại phát triển một điện thế. Trong trường hợp kim loại bị ăn mòn, khi nhiều phản ứng xảy ra đồng thời, điện thế này được gọi là điện thế hỗn hợp hoặc điện thế ăn mòn. Dãy điện hóa, được minh họa trong Bảng 1, dựa trên các giá trị điện thế ăn mòn này. Hình 1 trình bày điện thế ăn mòn cho nhiều kim loại và hợp kim khác nhau khi ngâm trong nước biển. Điện thế ăn mòn thay đổi tùy theo khả năng phản ứng của kim loại cụ thể. Ví dụ, kẽm có điện thế ăn mòn thấp hơn (âm hơn) có điện thế cao hơn sắt, xếp nó dưới sắt trong dãy Galvanic.
Hình 1: Dãy điện hóa của các kim loại cụ thể khi tiếp xúc với nước biển. Hình bao gồm các thanh ngang biểu thị phạm vi điện thế ăn mòn cho từng kim loại, được đo bằng vôn (V). Các phép đo này được tham chiếu so với điện cực calomel chuẩn (SCE, ở thang dưới) hoặc điện cực hydro chuẩn (SHE, ở thang trên).
Tiềm năng ăn mòn chịu ảnh hưởng của tất cả các phản ứng diễn ra trên bề mặt kim loại. Do đó, nó phụ thuộc vào một số yếu tố, chẳng hạn như thành phần chất điện phân và nồng độ oxy hòa tan. Trong Hình 1, tiềm năng ăn mòn của mỗi kim loại được mô tả dưới dạng một phạm vi giá trị chứ không phải là một giá trị duy nhất do ảnh hưởng của các yếu tố này. Hơn nữa, do những biến thể này, các nguồn khác nhau của chuỗi galvanic có thể biểu thị sự khác biệt trong trình tự của các kim loại.
Các bảng hoặc biểu đồ minh họa chuỗi galvanic đôi khi có thể có thép không gỉ và một số hợp kim khác ở hai vị trí. Một vị trí, thường được dán nhãn là ‘thụ động’, tương ứng với hành vi của hợp kim trong điều kiện bình thường. Điều này phù hợp với vị trí của thép không gỉ, như thể hiện trong Bảng 1 và Hình 1. Vị trí thứ hai, được chỉ định là ‘chủ động’, thấp hơn trong chuỗi galvanic và áp dụng khi lớp màng bảo vệ thụ động của hợp kim bị phá vỡ, điều này có thể xảy ra trong các tình huống ăn mòn hố và khe hở.
Ăn mòn kim loại do tiếp xúc
Khi hai kim loại, chẳng hạn như bạc và sắt, tiếp xúc trong môi trường điện phân, chúng trải qua một quá trình cân bằng điện thế điện hóa của chúng. Sự cân bằng này ổn định ở một giá trị giữa điện thế ăn mòn của hai kim loại, dẫn đến sự thay đổi tốc độ ăn mòn của chúng. Trong trường hợp này, kim loại phản ứng mạnh hơn, sắt, bị ăn mòn nhanh hơn so với tốc độ ăn mòn độc lập của nó, trong khi kim loại quý hơn, bạc, bị ăn mòn chậm hơn so với khi nó độc lập. Đồng thời, tốc độ của các phản ứng catốt, chẳng hạn như phản ứng oxy, trải qua những thay đổi ngược lại; chúng tăng tốc trên kim loại quý hơn và giảm tốc trên kim loại hoạt động mạnh hơn. Sự ăn mòn gia tăng này của kim loại hoạt động mạnh hơn, được minh họa bằng sắt trong trường hợp này, thường được gọi là ăn mòn galvanic. Tuy nhiên, bản thân dãy galvanic không định lượng được mức độ thay đổi tốc độ ăn mòn này, mặc dù nó thường rõ rệt hơn khi các kim loại được đặt cách xa nhau trong dãy galvanic.
Hình 2 cung cấp một ví dụ minh họa về các phản ứng này, trong đó lớp mạ bạc đã bị phá vỡ, để lộ lớp sắt bên dưới. Trong trường hợp này, sự ăn mòn được khuếch đại bởi diện tích bề mặt tương đối của hai kim loại, trong đó lớp bạc lộ ra cung cấp một diện tích đáng kể để oxy tham gia vào quá trình ăn mòn.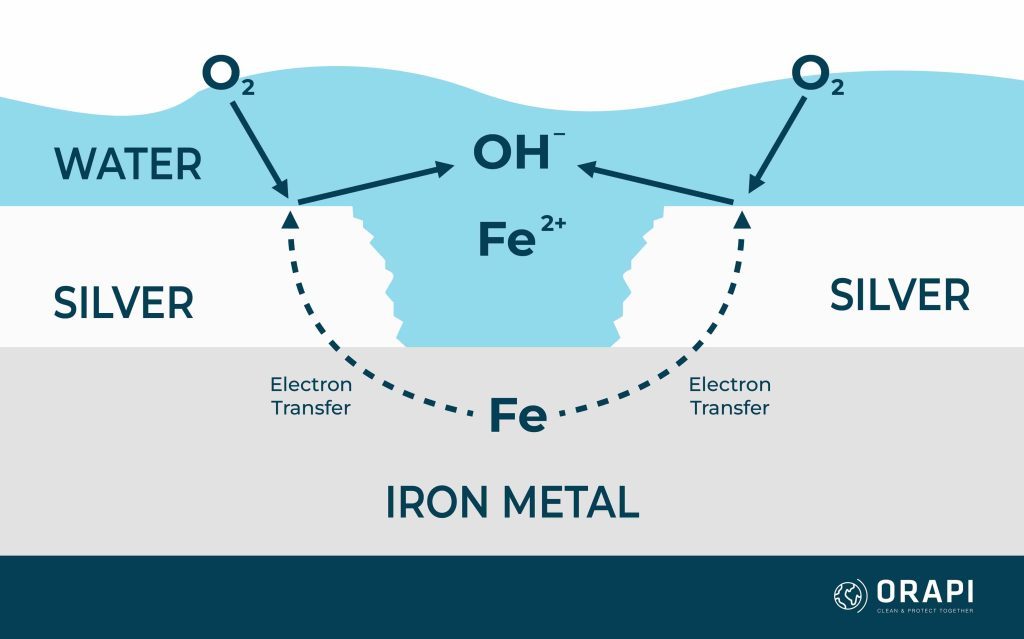
Mặt có lợi của ăn mòn điện hóa
Mạ hoạt động
Ăn mòn điện hóa xảy ra khi một kim loại được mạ lên kim loại khác. Hành vi ăn mòn được xác định bởi hoạt động tương đối của hai kim loại, cụ thể là kim loại mạ và kim loại bên dưới. Một ví dụ về điều này có thể thấy ở thép mạ kẽm, trong đó một lớp kẽm được phủ lên thép, khiến kim loại mạ hoạt động mạnh hơn.
Thép phủ kẽm được bảo vệ theo hai cách: thông qua rào cản vật lý và ăn mòn điện hóa. Nếu lớp kẽm vẫn còn nguyên vẹn, nó hoạt động như một rào cản chống lại độ ẩm, ngăn thép bị ăn mòn. Kẽm, mặc dù hoạt động mạnh hơn thép, được bảo vệ bởi các sản phẩm ăn mòn của nó, thường là kẽm cacbonat, làm chậm quá trình ăn mòn của nó ở ngoài trời. Tuy nhiên, nếu lớp kẽm bị trầy xước hoặc hư hỏng theo bất kỳ cách nào, thép sẽ bị lộ ra và kẽm sẽ bị ăn mòn ưu tiên, do đó bảo vệ thép khỏi bị ăn mòn điện hóa.
Thép mạ kẽm cung cấp khả năng bảo vệ chống lại ăn mòn điện hóa, nhờ sự hiện diện của kẽm. Tuy nhiên, khi thép mạ kẽm được sử dụng cùng với các kim loại khác, vị trí của kẽm bên dưới hầu hết các kim loại khác trong chuỗi điện hóa có thể dẫn đến ăn mòn kẽm nhanh chóng. Điều này có thể khiến thép dễ bị tổn thương khi hầu hết kẽm đã bị ăn mòn.
Thép có thể được bảo vệ bằng nhôm và cadmium, là những chất có hàm lượng thấp hơn trong chuỗi mạ điện. Ngoài ra, thép có thể được phủ bằng hợp kim nhôm và kẽm. Tuy nhiên, việc sử dụng cadmium để mạ phần cứng bằng thép trên đồ nội thất đã giảm do độc tính của nó.
Mạ cao cấp
Phủ một kim loại hoạt động mạnh hơn bằng một kim loại quý hơn là một phương pháp phổ biến để đạt được vẻ ngoài của kim loại quý hơn. Ví dụ, các tác phẩm điêu khắc làm bằng kẽm có thể được mạ đồng, lan can cầu thang bằng đồng thau có thể được mạ crom và khay đồng có thể được mạ bạc. Vàng cũng có thể được mạ lên bạc hoặc hợp kim đồng để tạo ra các vật phẩm tôn giáo dát vàng. Thép có thể được mạ bằng nhiều kim loại khác nhau, chẳng hạn như hợp kim đồng cho khung giường bằng đồng thau, bạc cho đồ dùng nhà bếp, crom cho các bộ phận ô tô, thiếc cho lon mạ thiếc và niken, trước khi phủ một lớp crom lên trên. Miễn là lớp phủ liên tục và không có lỗ rỗng, chỉ có kim loại quý hơn mới được tiếp xúc, đóng vai trò như một rào cản bảo vệ kim loại bên dưới khỏi bị ăn mòn. Nếu kim loại quý hơn bị ăn mòn chậm, khả năng bảo vệ của nó có thể kéo dài trong thời gian dài.
Khi lớp mạ kim loại bị lỗi hoặc hư hỏng, kim loại bên dưới có thể bị ăn mòn. Ăn mòn điện hóa, trong trường hợp này, không cung cấp bất kỳ khả năng bảo vệ nào, thay vào đó, nó làm tăng tốc độ ăn mòn của kim loại bên dưới. Ví dụ, các tác phẩm điêu khắc kẽm mạ đồng có thể bị rỗ nghiêm trọng xung quanh các khuyết điểm trong lớp mạ đồng do sự ăn mòn điện hóa của kẽm, đặc biệt là ở ngoài trời. Tương tự như vậy, “lon thiếc” làm bằng thép mạ thiếc cũng có thể bị ăn mòn điện hóa của thép bên dưới nếu lớp thiếc bị hỏng. Sự ăn mòn tập trung của kim loại bên dưới có thể dẫn đến việc nâng lớp mạ nếu nó xảy ra ở một khu vực nhỏ.
Trong một số trường hợp, có thể xảy ra hiện tượng mạ vô ý, dẫn đến ăn mòn điện hóa. Ví dụ, nếu đài phun nước có tác phẩm điêu khắc bằng nhôm chứa các ion đồng từ ống đồng, đồng có thể lắng đọng trên nhôm do lớp mạ thay thế điện hóa. Các khu vực mà đồng đã mạ sau đó có thể gây ra sự ăn mòn điện hóa của nhôm ở các khu vực không mạ, dẫn đến rỗ. Vấn đề tương tự này cũng có thể phát sinh khi mạ đồng lên kẽm. Cần lưu ý rằng ngay cả một lượng nhỏ ion đồng trong nước (ít nhất là 0,1 ppm) cũng có thể làm tăng tốc độ ăn mòn của kẽm.
Xử lý ăn mòn điện hóa
Chọn kim loại tương thích
Khi hai kim loại không giống nhau tiếp xúc, nên chọn kim loại được đặt càng gần nhau càng tốt trong chuỗi mạ điện. Ví dụ, nếu lựa chọn ban đầu cho phần khung bên trong tác phẩm điêu khắc bằng đồng là thép, thì nên thay thế bằng thép không gỉ, một kim loại được xếp hạng cao hơn trong Bảng 1 của chuỗi mạ điện.
Vật liệu cách điện
Để ngăn ngừa ăn mòn mạ điện, một lựa chọn là sử dụng chất cách điện như Teflon hoặc nhựa để tách các kim loại khác nhau. Ví dụ, một tác phẩm điêu khắc bằng kim loại quý hơn có thể có phần khung kim loại hoạt động mạnh hơn. Tuy nhiên, nếu có nhiều vùng tiếp xúc, chỉ cần một vùng tiếp xúc bị hỏng cũng có thể khiến hai kim loại tiếp xúc với nhau về mặt điện. Ngoài ra, nếu chất cách điện trở nên xốp theo thời gian, nó có thể giữ lại chất điện phân như một miếng bọt biển. Điều này đã được chứng kiến ở Tượng Nữ thần Tự do, nơi các bộ tách amiăng ngâm trong vecni trở nên xốp theo thời gian. Là một phần của chương trình bảo trì, điều quan trọng là phải thường xuyên kiểm tra các chất cách điện giữa các kim loại để ngăn ngừa ăn mòn mạ điện.
Vật thể mạ
Khi hai kim loại được mạ cùng nhau, chúng không thể tách rời. Vật thể sẽ bị lỗi nếu lớp mạ đặt kim loại quý hơn lên trên. Nguyên nhân là do vấn đề ăn mòn điện hóa đã nằm sẵn trong chính vật thể đó. Giải pháp duy nhất là giữ vật thể trong môi trường không gây ra hiện tượng ăn mòn điện hóa. Vì các kim loại được kết nối cố định thông qua kết nối điện nên việc tránh bất kỳ kết nối nào thông qua chất điện phân là rất quan trọng. Cách tốt nhất là bảo quản vật thể trong môi trường khô ráo hoặc bảo vệ bằng lớp sáp thường xuyên hoặc các lớp phủ khác.
Đe dọa đến tính toàn vẹn của cấu trúc
Nếu ăn mòn điện hóa đe dọa đến tính toàn vẹn của cấu trúc vật thể, thì cần loại bỏ lớp ăn mòn hoặc thay thế các bộ phận bị ăn mòn. Đây có thể là một nhiệm vụ đầy thách thức, đặc biệt là đối với các tác phẩm điêu khắc lớn. Tuy nhiên, bằng cách sử dụng chất tẩy ăn mòn thích hợp, bạn có thể khôi phục kim loại về hình dạng ban đầu.